Co to jest?
Liposomy są zamkniętymi strukturami pęcherzykowymi, które mogą mieścić się w zakresie od 20-25 nm do 2, 5 μm (lub 2500 nm). Ich struktura (bardzo podobna do struktury błon komórkowych) charakteryzuje się obecnością jednej lub więcej podwójnych warstw lipidów amfifilowych, które ograniczają hydrofilowy rdzeń, w którym znajduje się materiał w fazie wodnej. Ponadto faza wodna jest również obecna na zewnątrz liposomów.
Zainteresowanie tym odkryciem było natychmiast duże, szczególnie w dziedzinie medyczno-farmaceutycznej. Nic dziwnego, że od lat 70. liposomy były używane, w formie eksperymentalnej, jako pojazdy farmaceutyczne. Stopniowo naukowcy nauczyli się doskonalić właściwości liposomów, aby móc wywierać pożądany efekt terapeutyczny.
Badania w tej dziedzinie były i nadal są bardzo intensywne, więc nie jest zaskakujące, że liposomy są obecnie stosowane jako skuteczne systemy dostarczania leków.
struktura
Struktura i właściwości liposomów
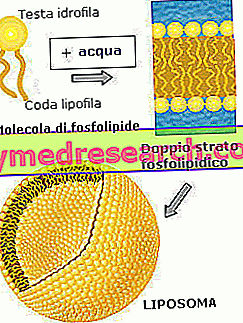
Jak wspomniano, liposomy mają strukturę, która charakteryzuje się obecnością jednej lub więcej podwójnych warstw lipidów amfifilowych. Szczegółowo, te podwójne warstwy są w większości utworzone przez cząsteczki fosfolipidów: te z warstwy zewnętrznej są regularnie umieszczane obok siebie i eksponują swoją głowę polarną (hydrofilową część cząsteczki) w otaczającym je wodnym środowisku; apolarny ogon (hydrofobowa część cząsteczki) jest zamiast tego zwrócony do wewnątrz, gdzie przeplata się z tym z drugiej warstwy lipidowej, która ma organizację odzwierciedlającą poprzednią. W rzeczywistości, w wewnętrznej warstwie fosfolipidowej, głowy polarne są zwrócone w stronę środowiska wodnego zawartego w jamie liposomowej.
Dzięki tej szczególnej strukturze liposomy mogą pozostać zanurzone w fazie wodnej, jednocześnie mieszcząc w sobie zawartość wodną, w której można rozpraszać składniki czynne lub inne cząsteczki.
Jednocześnie - dzięki podwójnej warstwie fosfolipidów - zapobiega się wchodzeniu i wychodzeniu cząsteczek wody lub cząsteczek polarnych, skutecznie izolując zawartość liposomu (którego nie można zmodyfikować przez wejście lub wyjście) wody lub polarnych substancji rozpuszczonych).

niosomach
Niosomy ( liposomy niejonowe) są specjalnymi liposomami, których struktura różni się od „klasycznych” liposomów. W rzeczywistości, w niosomach warstwy fosfolipidowe są zastępowane przez niejonowe lipidy syntezy amfifilowej, zazwyczaj dodawane do cholesterolu. Niosomy są mniejsze niż 200 nanometrów, są bardzo stabilne i mają różne szczególne cechy, które - między innymi - czynią je bardzo odpowiednimi do stosowania miejscowego.
funkcje
Charakterystyka liposomów zależy od typowej struktury, do której te pęcherzyki są wyposażone. Warstwy zewnętrzne mają w rzeczywistości niezwykłe powinowactwo do błon plazmatycznych, których zarysują w szerokim zakresie skład (naturalne fosfolipidy, takie jak fosfatydylocholina, fosfatydyloetanoloamina i estry cholesterolu).
W ten sposób rozpuszczalne w wodzie substancje zawarte w mikrosferach liposomowych mogą być łatwo przenoszone do komórek.
Jednocześnie liposom może również włączać farmakologicznie aktywne cząsteczki lipofilowe do swojej zewnętrznej dwuwarstwy fosfolipidowej.
Ponadto, jak wspomniano, właściwości liposomów można poprawić w celu dostosowania pęcherzyków do najbardziej zróżnicowanych wymagań. Aby to zrobić, należy interweniować, wprowadzając zmiany strukturalne różnego rodzaju w zależności od celu, który ma zostać osiągnięty: na przykład problem związany z niestabilnością fosfolipidów (wysoka tendencja do utleniania), można rozwiązać przez częściowe uwodornienie, dodatek przeciwutleniacza (alfa-tokoferol) lub przez zastosowanie liofilizacji (proliposomy), co pozwala na zachowanie stabilności pęcherzyków przez bardzo długi czas.
Ponadto, podwójna warstwa lipidowa może być skonstruowana tak, aby zwiększyć wiązanie do pewnych typów komórek, na przykład przez przeciwciała, lipidy lub węglowodany. W ten sam sposób powinowactwo liposomów do danej tkanki można modyfikować przez zmianę składu i ładunek elektryczny (przez dodanie stearyloaminy lub pęcherzyków fosfatydyloseryny z ładunkiem dodatnim, podczas gdy z fosforanem detylu uzyskuje się ładunki ujemne), co zwiększa stężenie leku w narządzie docelowym.
Wreszcie, w celu zwiększenia okresu półtrwania liposomów, możliwa jest modyfikacja powierzchni przez sprzężenie cząsteczek glikolu polietylenowego (PEG) z dwuwarstwą lipidową, wytwarzając tak zwane „ liposomy stealth ”. Zatwierdzona przez FDA terapia lekami na raka wykorzystuje powlekane PEG liposomy, które transportują doksorubicynę. Jak stwierdzono powyżej, powłoka ta znacznie wydłuża okres półtrwania liposomów, które stopniowo koncentrują się w komórkach rakowych przenikających naczynia włosowate guza; te, które w rzeczywistości powstały niedawno, są bardziej przepuszczalne niż te w zdrowych tkankach i jako takie umożliwiają liposomom gromadzenie się w tkance nowotworowej i uwalnianie tutaj składników aktywnych toksycznych dla komórek rakowych.
zastosowania
Zastosowania i zastosowania liposomów
Dzięki swoim szczególnym cechom i strukturom liposomy są wykorzystywane w różnych dziedzinach: od medycznej i farmaceutycznej po czysto kosmetyczne. W rzeczywistości, ponieważ liposomy mają wysokie powinowactwo do warstwy rogowej naskórka, są intensywnie stosowane w tym obszarze, aby sprzyjać wchłanianiu przez skórę substancji funkcjonalnych.
Jeśli chodzi o dziedzinę medycyny i farmacji, zamiast tego liposomy znajdują zastosowanie zarówno w dziedzinie terapeutycznej, jak i diagnostycznej.
W szczególności zdolność liposomów do izolowania ich zawartości ze środowiska zewnętrznego jest szczególnie użyteczna w przenoszeniu substancji podatnych na degradację (takich jak na przykład białka i kwasy nukleinowe).
Jednocześnie liposomy można wykorzystać do zmniejszenia toksyczności niektórych leków: tak jest na przykład w przypadku doksorubicyny - leku przeciwnowotworowego wskazanego w raku jajnika i prostaty - który jest zamknięty w liposomach o długim krążeniu znacznie zmodyfikowała farmakokinetykę, a także poprawiła stopień skuteczności i toksyczności.
klasyfikacja
Klasyfikacja i typy liposomów
Klasyfikację liposomów można przeprowadzić według różnych kryteriów, takich jak: wymiary, struktura (liczba podwójnych warstw lipidowych, z których składa się liposom) i przyjęta metoda przygotowania (ta ostatnia klasyfikacja nie zostanie jednak uwzględniona w kurs artykułu).
Te klasyfikacje i główne typy liposomów zostaną krótko opisane poniżej.
Klasyfikacja oparta na kryteriach strukturalnych i wymiarowych
W zależności od struktury i liczby podwójnych warstw fosfolipidów, w które wyposażony jest każdy pęcherzyk, można podzielić liposomy na:
Liposomy jednowarstwowe
Jednowarstwowe liposomy składają się z pojedynczej dwuwarstwy fosfolipidowej, która zamyka hydrofilowy rdzeń.
W zależności od ich wielkości, liposomy jednowarstwowe można dalej podzielić na:
- Małe pęcherzyki jednowarstwowe lub SUV ( małe pęcherzyki jednowarstwowe ), których średnica może zmieniać się od 20 nm do 100 nm;
- Duże pęcherzyki jednowarstwowe lub LUV ( duże pęcherzyki jednowarstwowe ), których średnica może zmieniać się od 100 nm do 1 μm;
- Olbrzymie jednowarstwowe pęcherzyki lub GUV ( pęcherzyki gigantyczne jednowarstwowe ), których średnica jest większa niż 1 μm.
Liposomy wielowarstwowe
Liposomy wielowarstwowe lub MLV ( pęcherzyki wielolamelarne ) są bardziej złożone, ponieważ charakteryzują się koncentryczną obecnością różnych warstw lipidowych (na ogół więcej niż pięć), oddzielonych od siebie fazami wodnymi (struktura skóry cebuli). W przypadku tej szczególnej cechy liposomy wielowarstwowe osiągają średnice w zakresie od 500 do 10 000 nm. Dzięki tej technice możliwe jest kapsułkowanie większej liczby lipofilowych i hydrofilowych składników aktywnych.
Do grupy liposomów wielowarstwowych należą również tak zwane liposomy oligolamellos lub OLV ( OligoLamellar Vesicles ), zawsze składające się z szeregu koncentrycznych podwójnych warstw fosfolipidów, ale o mniejszej liczbie w porównaniu z „prawidłowymi” liposomami wielowarstwowymi.
Liposomy wielopunktowe
Wielokomórkowe liposomy lub MVV ( pęcherzykowe pęcherzyki ) charakteryzują się obecnością podwójnej warstwy fosfolipidowej, w której znajdują się inne liposomy, które jednak nie są koncentryczne, jak w przypadku liposomów wielowarstwowych.
Inne klasyfikacje
Oprócz tego, co do tej pory zaobserwowano, możliwe jest przyjęcie innego systemu klasyfikacji, który dzieli liposomy na:
- Liposomy wrażliwe na PH : są to pęcherzyki, które uwalniają swoją zawartość w lekko kwaśnych środowiskach. W rzeczywistości przy pH 6, 5 lipidy, które je tworzą, protonują i sprzyjają uwalnianiu leku. Ta cecha jest użyteczna, ponieważ bardzo często na poziomie mas guza występuje znaczące obniżenie pH, ze względu na tkankę martwiczą, która tworzy się wraz ze wzrostem guza.
- Liposomy wrażliwe na temperaturę : uwalniają swoją zawartość w temperaturze krytycznej (zazwyczaj około 38-39 ° C). W tym celu po podaniu liposomów obszar, w którym obecna jest masa guza, jest ogrzewany, na przykład za pomocą ultradźwięków.
- Immunoliposomy : uwalniają swoją zawartość, gdy wchodzą w kontakt z komórką, która ma określony antygen.
Zalety i wady
Główne zalety i wady liposomów
Zastosowanie liposomów ma wiele znaczących zalet, takich jak:
- Składniki zewnętrznych warstw fosfolipidów są biokompatybilne, więc nie powodują niepożądanych efektów toksycznych lub alergicznych;
- Jestem w stanie włączyć zarówno cząsteczki hydrofilowe, jak i lipofilowe do tkanek docelowych;
- Przenoszone substancje są chronione działaniem enzymów (proteaz, nukleaz) lub środowisk denaturujących (pH);
- Są w stanie zmniejszyć toksyczność toksycznych lub drażniących środków;
- Można je podawać różnymi drogami (doustnie, pozajelitowo, miejscowo itp.);
- Mogą być syntetyzowane w taki sposób, aby zwiększyć ich powinowactwo do konkretnych miejsc docelowych (białek, tkanek, komórek itp.);
- Są biodegradowalne, wolne od toksyczności i mogą być obecnie przygotowywane na dużą skalę.




